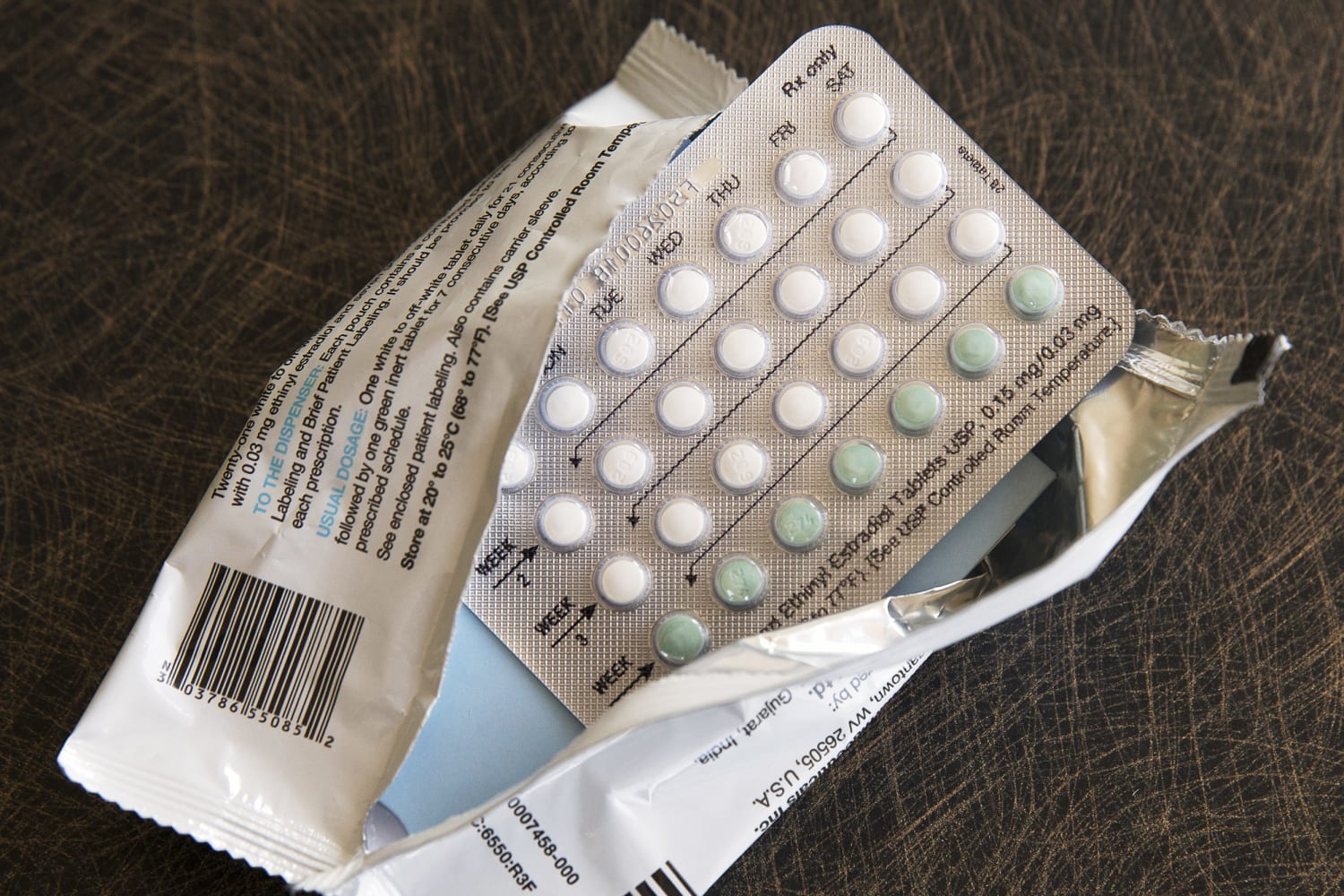
El viernes, los científicos de la Administración de Drogas y Alimentos expresaron su escepticismo acerca de si la píldora anticonceptiva puede reemplazarse con una receta de venta libre.
La evaluación por parte del personal de la FDA, incluida en documentos de antecedentes publicado el viernes, se produce antes de una reunión de dos días programada para la próxima semana cuando los asesores de la agencia votarán si recomiendan que la agencia permita la venta sin receta de una píldora anticonceptiva llamada Opill.
Si los asesores lo recomiendan y la FDA aprueba el uso de Opill sin receta, sería la primera vez que la píldora podría venderse sin receta. HRA Pharma, que fabrica Opill, espera que la agencia pueda tomar una decisión final a fines del verano.
La principal preocupación de los científicos de la FDA parecía ser que las mujeres pudieran seguir la etiqueta de instrucciones del paquete y tomar el medicamento correctamente, quienes dudaban que el fabricante de la píldora hubiera proporcionado suficientes datos.
Las píldoras anticonceptivas deben tomarse a la misma hora todos los días. No hacerlo podría conducir a un embarazo no deseado, escribieron los científicos de la agencia. Pero omitir dosis no es poco común: estudios presentado que aproximadamente la mitad de las mujeres reportan omitir una dosis al menos una vez al mes.
la FDA aprobado Opill para uso con receta en 1973. Como parte de la solicitud de la compañía para uso sin receta, la agencia solicitó información adicional sobre la efectividad del medicamento en la población actual.
Sin embargo, el análisis actualizado proporcionado por la compañía se quedó corto, dijeron los científicos de la FDA, y señalaron que se basaba en estudios de baja calidad, muchos de los cuales databan de las décadas de 1960 y 1970.
El personal de la FDA también cuestionó los resultados de otro estudio, llamado Access, en el que los investigadores evaluaron si los participantes tomaron el medicamento según las instrucciones de la etiqueta. El estudio encontró que alrededor del 97% de las veces, los participantes dijeron que tomaron el medicamento correctamente o siguieron las instrucciones de la etiqueta si se saltaban una dosis.
La agencia, sin embargo, dijo que encontró que «una parte sustancial» de los participantes sobrestimó la cantidad de píldoras que tomaron o informaron haber tomado más píldoras de las que se dispensaron, factores que «cuestionan la confiabilidad de cualquier dato sobre el uso real».
Un impulso para un mayor acceso al control de la natalidad
En una declaración emitida en respuesta a los documentos informativos de la FDA, un vocero de Perrigo, propietario de HRA Pharma, argumentó que Opill es seguro y eficaz para su uso sin receta.
«El control de la natalidad diario se aprobó hace más de 60 años y las píldoras de progestágeno solo tienen un largo historial como método seguro y eficaz para prevenir el embarazo», dijo el vocero. «Esperamos presentar nuestros datos y tener una discusión significativa sobre estos temas el 9 y 10 de mayo».
El impulso para un acceso más fácil al control de la natalidad se produce en medio de un panorama político cambiante para los derechos reproductivos de las mujeres.
En junio pasado, la Corte Suprema anuló la decisión histórica Roe v. Wade que garantizaba el derecho constitucional al aborto. En abril, la Corte Suprema anuló la decisión de un tribunal inferior de emitir una orden judicial a nivel nacional sobre el fármaco mifepristona, uno de los dos fármacos utilizados en los abortos médicos. Ese caso aún está pendiente en los tribunales inferiores, y el Quinto Circuito está programado para escuchar los argumentos orales el 17 de mayo.
HRA Pharma está solicitando a la FDA que apruebe la píldora anticonceptiva de venta libre para todas las mujeres en edad fértil.
Hacer que la píldora esté disponible sin restricciones de edad podría ser especialmente importante para los jóvenes adolescentes y adultos que a menudo tienen muchas barreras para acceder a la atención médica y obtener recetas para el control de la natalidad, Dra. Kristyn Brandi, miembro del Colegio Estadounidense de Obstetras y Ginecólogos. . Entre las jóvenes de 15 a 17 años en los Estados Unidos, el 72 % de los embarazos no fueron planeados, según datos proporcionados por la FDA.
Otros anticonceptivos, como los preservativos, implican la participación activa de la pareja de la mujer.
Brandi se negó a comentar sobre los hallazgos de la FDA en los materiales informativos.
En los documentos del viernes, la FDA señaló que, en un entorno de prescripción, se ha demostrado que los medicamentos que solo contienen progestina son seguros. La agencia señaló que existe un riesgo de cáncer de mama y sangrado vaginal no diagnosticados, y dijo que planea preguntar a los paneles asesores la próxima semana si creen que los consumidores podrán evaluar por sí mismos estos riesgos de seguridad. (Estos riesgos son comunes entre los anticonceptivos hormonales).
El personal de la agencia también señaló que faltaba información sobre el uso en adolescentes y si podían seguir las instrucciones de la etiqueta.